脂溢性皮炎(Seborrhoeic dermatitis,SD)是一种常见的慢性炎症性皮肤病,在一般人群中的患病率约为 3%,在免疫抑制或神经系统疾病患者中更高,其病因包括马拉色菌过度生长和宿主免疫异常等。本文简要介绍了 SD 的发病机制、临床病理改变和治疗。
1. 发病机制
马拉色菌在 SD 发病中起到重要作用,但不是直接和唯一的原因,证据包括在皮损中未发现致病性菌丝,在马拉色菌生长旺盛的夏季皮损反而减轻。内源性因素如皮脂的质、量改变及皮肤屏障缺陷可能为该菌过度定植提供了良好的条件。近年来发现参与 SD 发病的因素还包括:
(1)宿主免疫失衡:有些类型的免疫细胞抑制可能导致其他免疫细胞更活跃而促进 SD 发病,例如在艾滋病、丙型肝炎、器官移植或某些恶性肿瘤患者中 SD 发病率和严重度更高。
(2)菌群失调:除了马拉色菌以外,还观察到金黄色葡萄球菌定植增加、葡萄球菌/丙酸杆菌属失衡。
(3)神经内分泌活性异常:已观察到 SD 在高泌乳素血症、帕金森病、癫痫、脑外伤、面瘫、脑梗死患者中的发病率升高
(3)皮脂腺活性增加和表皮屏障受损。
2. 临床特征
SD 的发病率有 3 个高峰,分别为出生后 2 周至 12 个月、青春期、30~60 岁。在婴儿期,SD 表现为头皮油腻的黄色结痂,称为「摇篮帽」;在青少年和成人中则表现为皮脂溢出部位如头皮、面部(眉、鼻唇沟、上唇)(见图 1A~B)、耳、耳后和上胸部油腻的黄色鳞屑伴红斑。
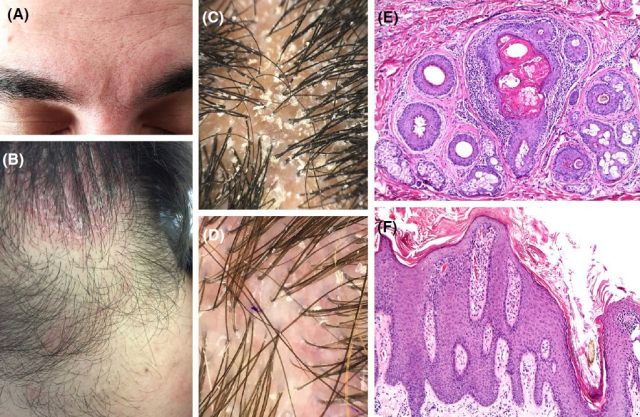
图 1.(A~B)眉和头皮红斑、脱屑;(C~D)毛发镜示毛囊内鳞屑;(E)漏斗水平水平切片示扩张的皮脂腺导管内充满皮脂,可见角化不全;(F)银屑病样棘层肥厚和轻度血管周围淋巴细胞浸润(来源:Wikramanayake 等 2019)
SD 严重度变异较大,从皮脂溢出部位轻度红斑和细碎脱屑,到浸润性斑块伴黄色结痂,再到免疫抑制患者的广泛性损害(见图 2),甚至出现潜在性危及生命的剥脱性红皮病。有时同时存在 SD 与银屑病的症状,称为脂溢性银屑病(Sebopsoriasis)。
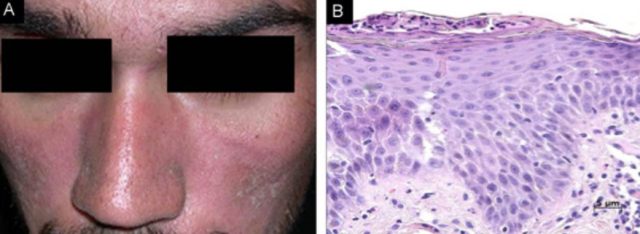
图 2.(A)HIV 患者显示头皮和面部皮脂溢出部位以丘疹鳞屑为主的损害;(B)组织病理示局灶性角化不全、中度棘层肥厚、海绵水肿和散在中性粒细胞浸润(来源:Cedeno-Laurent 等 2011)
SD 患者的脱屑、暴露部位如面或耳部皮肤发红、头屑增多、瘙痒以及 SD 本身的慢性复发性病程影响了患者的生活质量和自尊心。
3. 组织病理
SD 的病理改变无特异性,急性期和慢性期表现不同,急性期主要为毛囊和血管周围炎症,常可见海绵水肿、银屑病样增生以及围绕毛囊口的角化不全和毛囊角栓(见图 1E),结痂边缘可见中性粒细胞。在慢性期,银屑病样增生更明显,海绵水肿轻微(见图 1F)。
4. 治疗
SD 的自然过程为慢性和复发性,治疗目的是控制症状而非根治。由于马拉色菌过度增殖、局部刺激和炎症在 SD 中的重要作用,常用治疗药物为外用抗真菌剂和抗炎药。
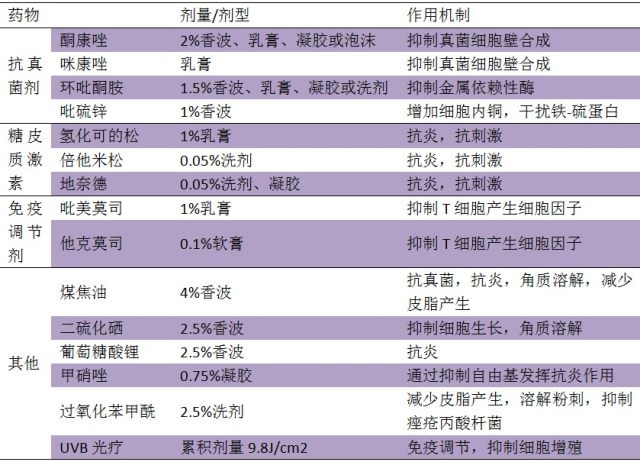
抗真菌剂如酮康唑可抑制马拉色菌生长,外用糖皮质激素和免疫调节剂抑制角质形成细胞和中性粒细胞产生的促炎细胞因子(IL-1α、IL-6、IL-8 和 TNFα),从而抑制皮肤炎症。表 1 总结了 SD 的常用外用疗法。
表 1. SD 的外用治疗
参考文献
[1] Borda LJ, Perper M, Keri JE. Treatment of seborrheic dermatitis: a comprehensive review. J Dermatology Treat, 2018, 1-12.
[2] Wikramanayake TC, Broda LJ, Miteva M, et al. Seborrheic dermatitis-looking beyond malassezia. Exp Dermatol, 2019, 28(9):991-1001.
[3] Cedeno-Laurent F, Gomez-Flores M, Mendez N, et al. New insights into HIV-1 primary skin disorders. J Int AIDS Soc, 2011,14:5.
